menu

Familles SMA
France
Familles SMA France (FSMA) est une association d'intérêt général qui a pour objet de faciliter le partage d'informations et de contribuer à la mise en place de stratégies thérapeutiques efficaces pour guérir l'Amyotrophie Spinale Infantile (SMA).


Conférence CureSMA - Orlando (USA) du 29/06 au 01/07/2017




L'un des membres de notre association, de passage à Orlando, a bien voulu nous transmettre un rapide compte-rendu de cet événement mondial qui regroupe autour des familles SMA, les chercheurs, les cliniciens et les laboratoires impliqués dans le domaine de la SMA.
En terme d'organisation, la conférence Cure SMA s'est partagée entre la partie "congrès scientifique" et la partie "rencontre familles SMA". De fait, en matière d'organisation il y avait une séparation nette entre le congrès scientifique et le congrès famille mais cette formule permet également une proximité et des échanges enrichissants entre scientifiques et patients/familles.
Les interventions des scientifiques ont été globalement assez brèves, concises et principalement consacrées à présenter l'état des lieux des travaux. C'était l'occasion de faire un tour d'horizon des différentes stratégies thérapeutiques du domaine de la SMA.
Cette conférence a été largement marquée par les 2 centres d'intérêt majeurs que sont Biogen, laboratoire américain qui produit et diffuse le premier traitement validé pour la SMA (nusinersen/spinraza) et Avexis, laboratoire américain également, pionnier et leader de la recherche du domaine de la thérapie génique.
Sachant que le spinraza/nusinersen bénéficie d'une Autorisation de mise sur le Marché aux USA depuis plus de six mois, le discours a été essentiellement tourné sur l'organisation du processus de prise en charge des injections intrathécales. Les patients américains sont donc invités à se rapprocher de leurs cliniciens afin de discuter, au cas par cas, de l'opportunité et des modalités pratiques d'un démarrage du traitement. A noter, également, que la mise à disposition récente du spinraza et son efficacité démontrée en particulier chez les nourrissons atteints de SMA type 1, conduisent les familles SMA américaines à envisager de demander la mise en place de tests de dépistage systématique de la SMA chez les nouveaux-nés. Un symposium spécifique à ce thème s'est déroulé pendant la conférence.
S'agissant d'Avexis, le projet de développement est en ligne avec leurs objectifs. Les premiers résultats des essais cliniques confirment l'intérêt de poursuivre ces études. Les experts présents sur place ont indiqué, également, que la fabrication des composants nécessaires à la mise en place de cette stratégie thérapeutique (virus), sera réalisée dans une usine localisée à Chicago, à partir de financements liés à une introduction en bourse.
En ce qui concerne ROCHE, ont été présentés les deux projets en cours : olesoxime et RG 7916. Pour l'olesoxime, nous avons eu confirmation que les premiers essais n'avaient pas permis d'atteindre le critère principal de résultat, nécessitant ainsi des études complémentaires (Oléos), ce qui entraine encore un délai supplémentaire avant une éventuelle Autorisation de Mise sur le Marché de l'olesoxime (AMM). (Nota : ces perspectives de plus en plus lointaines d'une AMM pour l'olesoxime interpellent Familles SMA France... et nous en profitons pour indiquer que cette situation nous semble maintenant inacceptable au regard des engagements de mise à disposition rapide que l'AFM nous avait promis lors de la vente du laboratoire Trophos à ROCHE).

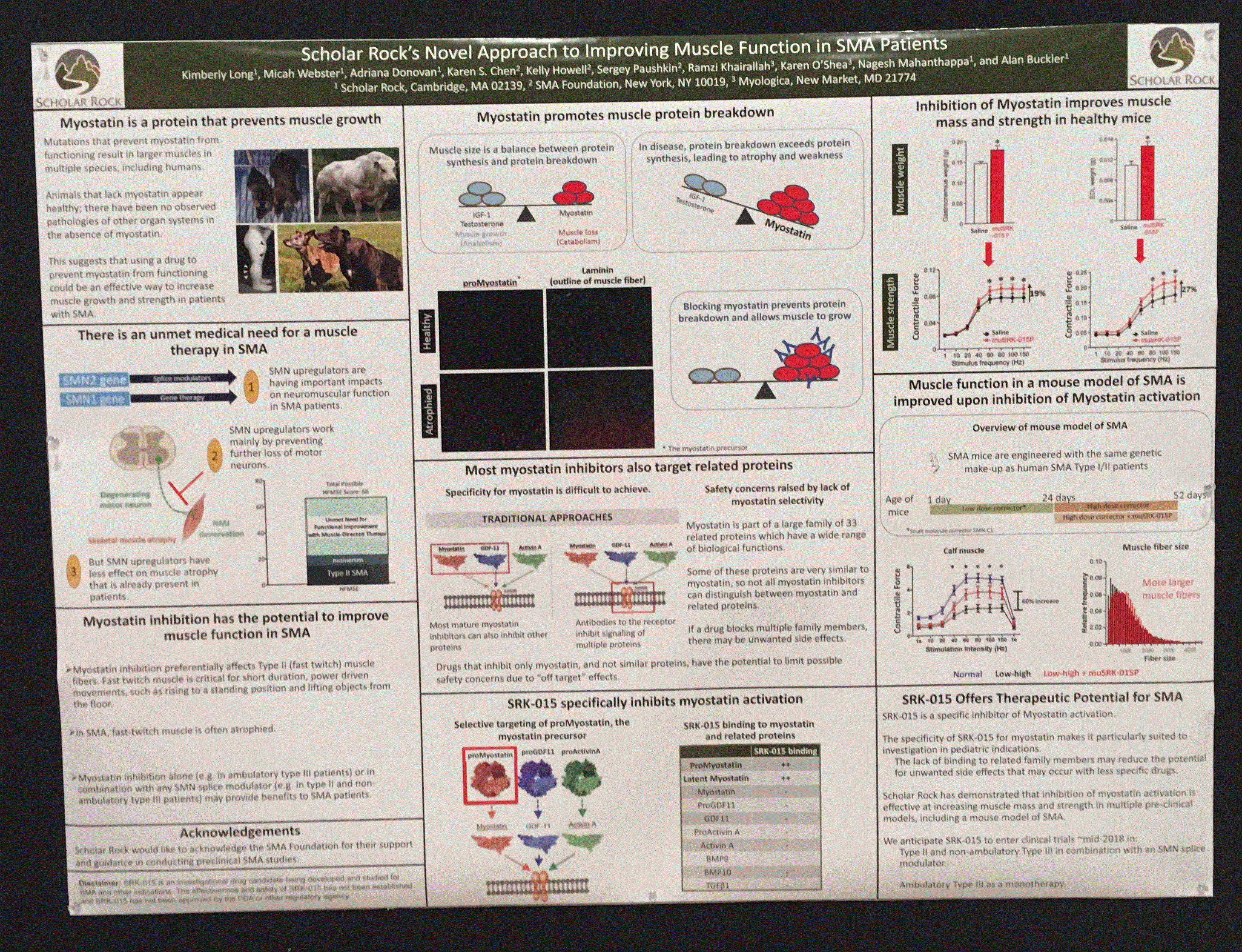
Une nouvelle approche pour améliorer les fonctions musculaires chez les patients SMA (Scholar Rock)


"Familles SMA France" est une association qui regroupe, en France, des familles concernées par l’amyotrophie spinale (SMA). La SMA reste la première maladie génétique aux conséquences mortelles chez les enfants de moins de deux ans. De plus, le caractère dégénératif de la maladie entraîne une perte inexorable des fonctions motrices conduisant à des situations de handicap très sévères.